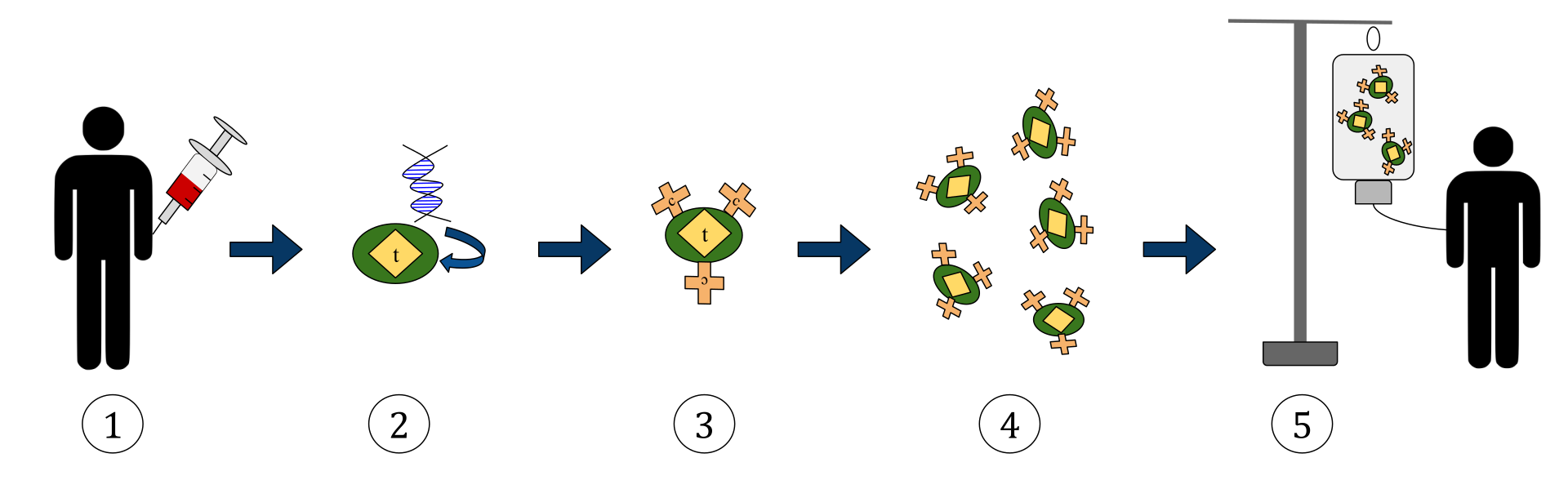
A fenti diagram a kiméra antigén receptor T-sejt terápia (CAR) folyamatát mutatja be. Ez az immunterápia egyik módszere, amely egyre nagyobb gyakorlat a rák kezelésében. A végeredmény olyan felszerelt T-sejtek termelése kell legyen, amelyek képesek felismerni a szervezetben lévő fertőzött rákos sejteket és leküzdeni azokat.
1. A T-sejteket (amelyeket „t”-vel jelölt tárgyak képviselnek) eltávolítják a páciens véréből.
2. Ezután laboratóriumi körülmények között a specifikus antigénreceptorokat kódoló gént beépítik a T-sejtekbe.
3. A CAR receptorok (c-vel jelölve) termelődése a sejtek felszínén.
4. Az újonnan módosított T-sejteket ezután tovább gyűjtik és tenyésztik a laboratóriumban.
5. Egy bizonyos idő elteltével a módosított T-sejteket visszajuttatják a páciensbe.
Kiméra antigén receptor T-sejtek (más néven CAR T-sejtek) olyan T-sejtek, amelyeket genetikailag úgy alakítottak ki, hogy mesterséges T-sejt-receptort állítsanak elő immunterápiában történő felhasználásra.
Kiméra antigén receptorok (AUTÓKmás néven kiméra immunreceptorok, kiméra T-sejt receptorokvagy mesterséges T sejt receptorok) olyan receptorfehérjék, amelyeket úgy alakítottak ki, hogy a T-sejteket új képességgel ruházzák fel egy adott fehérje megcélzására. A receptorok kimérák, mivel az antigénkötő és a T-sejt-aktiváló funkciókat egyetlen receptorban egyesítik.
A CAR-T sejtterápia CAR-okkal módosított T-sejteket használ a rákterápiában. A CAR-T immunterápia előfeltétele, hogy módosítsa a T-sejteket, hogy felismerjék a rákos sejteket, hogy hatékonyabban megcélozzák és elpusztítsák azokat. A tudósok T-sejteket gyűjtenek be az emberekből, genetikailag megváltoztatják azokat, majd a kapott CAR-T sejteket befecskendezik a betegekbe, hogy megtámadják daganataikat. A CAR-T-sejtek származhatnak a páciens saját vérében lévő T-sejtekből (autológ), vagy származhatnak egy másik egészséges donor T-sejtjéből (allogén). Miután izolált egy személytől, ezeket a T-sejteket genetikailag úgy alakítják át, hogy egy specifikus CAR-t expresszáljanak, ami programozza őket, hogy megcélozzanak egy, a daganatok felszínén jelenlévő antigént. A biztonság kedvéért a CAR-T sejteket úgy alakítják ki, hogy specifikusak legyenek egy olyan daganaton expresszálódó antigénre, amely nem expresszálódik egészséges sejtekben.
Miután a CAR-T sejteket beadták a betegbe, „élő gyógyszerként” hatnak a rákos sejtekkel szemben. Amikor érintkezésbe kerülnek a megcélzott antigénjükkel egy sejten, a CAR-T sejtek ahhoz kötődnek és aktiválódnak, majd szaporodnak és citotoxikussá válnak. A CAR-T sejtek több mechanizmuson keresztül pusztítják el a sejteket, beleértve a kiterjedt, stimulált sejtproliferációt, növelve más élő sejtekre mérgező hatásukat (citotoxicitás), valamint olyan tényezők fokozott szekrécióját idézve elő, amelyek hatással lehetnek más sejtekre, például citokinek, interleukinek és növekedési tényezők.
CAR-T sejtek termelése

A CAR-T sejtek termelésének első lépése a T-sejtek izolálása az emberi vérből. A CAR-T-sejtek előállíthatók a páciens saját véréből, amely autológ kezelésként ismert, vagy egy egészséges donor véréből, amelyet allogén kezelésként ismerünk. A gyártási folyamat mindkét esetben azonos; csak a kezdeti véradó kiválasztása különbözik.
Először is, a leukocitákat egy vérsejt-leválasztó segítségével izolálják a leukocita aferézis néven ismert eljárásban. A perifériás vér mononukleáris sejtjeit (PBMC) ezután elválasztják és összegyűjtik. A leukocita aferézis termékei ezután egy sejtfeldolgozó központba kerülnek. A sejtfeldolgozó központban a specifikus T-sejteket stimulálják, hogy azok aktívan szaporodjanak és nagy számban terjeszkedjenek. Terjeszkedésük elősegítésére a T-sejteket általában citokin interleukin 2-vel (IL-2) és anti-CD3 antitestekkel kezelik.
A felszaporodott T-sejteket megtisztítják, majd egy retrovirális vektoron keresztül transzdukálják a módosított CAR-t kódoló génnel, amely tipikusan vagy egy integrálódó gammaretrovírus (RV) vagy egy lentivírus (LV) vektor. Ezek a vektorok a modern időkben nagyon biztonságosak az U3 régió részleges törlése miatt. A CRISPR/Cas9 új génszerkesztő eszközt a közelmúltban retrovírus vektorok helyett használták, hogy a CAR gént a genom specifikus helyeibe integrálják.
A páciens limfodepléciós kemoterápián esik át a módosított CAR-T sejtek bejuttatása előtt. A keringő leukociták számának csökkenése a páciensben felszabályozza a termelődő citokinek számát, és csökkenti az erőforrásokért folytatott versengést, ami elősegíti a mesterséges CAR-T sejtek terjeszkedését.
Klinikai alkalmazások
2019 márciusáig világszerte mintegy 364 klinikai vizsgálat zajlott CAR-T-sejtek bevonásával. E vizsgálatok többsége a vérrákot célozza meg: a CAR-T-terápiák a hematológiai rosszindulatú daganatokkal kapcsolatos vizsgálatok több mint felét teszik ki. A CD19 továbbra is a legnépszerűbb antigéncélpont, ezt követi a BCMA (mieloma multiplexben általában kifejezve). 2016-ban a tanulmányok elkezdték feltárni más antigének, például a CD20 életképességét. A szolid daganatokkal kapcsolatos vizsgálatokban kevésbé dominál a CAR-T, a sejtterápián alapuló vizsgálatok körülbelül felében más platformokon, például NK-sejteken is részt vesznek.
Rák
A T-sejteket genetikailag úgy alakítják ki, hogy kiméra antigénreceptorokat expresszáljanak, amelyek specifikusan a páciens daganatsejtjein lévő antigének felé irányulnak, majd infundálják a páciensbe, ahol megtámadják és elpusztítják a rákos sejteket. A CAR-t expresszáló T-sejtek átadása ígéretes rákellenes terápia, mert A CAR-módosított T-sejtek úgy konstruálhatók, hogy gyakorlatilag bármilyen daganathoz kapcsolódó antigént megcélozzanak.
A korai CAR-T sejtkutatások a vérrákokra összpontosítottak. Az első jóváhagyott kezelések olyan CAR-okat alkalmaznak, amelyek a B-sejtes eredetű rákos megbetegedések, például az akut limfoblasztos leukémia (ALL) és a diffúz nagy B-sejtes limfóma (DLBCL) esetén jelen lévő CD19 antigént célozzák. Erőfeszítések vannak folyamatban számos más vérrák-antigént célzó CAR-k tervezésére is, beleértve a CD30-at a refrakter Hodgkin limfómában; CD33, CD123 és FLT3 akut mieloid leukémiában (AML); és BCMA myeloma multiplexben.
A szilárd daganatok nehezebb célpontot jelentettek. A jó antigének azonosítása kihívást jelent: ezeknek az antigéneknek erősen expresszálódnak a rákos sejtek többségén, de nagyrészt hiányoznak a normál szövetekben. A CAR-T-sejtek szintén nem jutnak hatékonyan a szilárd tumortömegek központjába, és az ellenséges daganat mikrokörnyezete elnyomja a T-sejt aktivitást.
Autoimmun betegség
Míg a legtöbb CAR T-sejt-vizsgálat egy olyan CAR T-sejt létrehozására összpontosít, amely képes kiirtani egy bizonyos sejtpopulációt (például a limfómasejteket célzó CAR T-sejteket), ennek a technológiának más felhasználási lehetőségei is vannak. A T-sejtek is megvédhetik a saját antigéneket az autoimmun reakcióktól. Egy CAR-val felszerelt szabályozó T-sejt potenciálisan toleranciát biztosíthat egy specifikus antigénnel szemben, ami hasznosítható szervátültetésben vagy reumás betegségekben, például lupuszban.
Satefy
Vannak súlyos mellékhatások, amelyek a szervezetbe kerülő CAR-T-sejtekből származnak, beleértve a citokin felszabadulási szindrómát és a neurológiai toxicitást. Mivel ez egy viszonylag új kezelés, kevés adat áll rendelkezésre a CAR-T sejtterápia hosszú távú hatásairól. Továbbra is aggodalomra ad okot a betegek hosszú távú túlélése, valamint a CAR-T sejtekkel kezelt nőbetegek terhességi szövődményei. Az anafilaxia várható mellékhatás, mivel a CAR idegen monoklonális antitesttel készül, és ennek eredményeként immunválaszt vált ki.
A célpont/tumoron kívüli felismerés akkor következik be, amikor a CAR-T sejt felismeri a megfelelő antigént, de az antigén egészséges, nem patogén szöveten expresszálódik. Ennek eredményeként a CAR-T sejtek megtámadják a nem daganatos szöveteket, például az egészséges B-sejteket, amelyek CD19-et expresszálnak. Ennek a káros hatásnak a súlyossága a támogató infúziókkal kezelhető B-sejtes aplasiától a halálhoz vezető rendkívüli toxicitásig változhat.
Valószínűtlen az is, hogy a módosított CAR-T sejtek maguk is rákos sejtekké alakulnak át inszerciós mutagenezis révén, mivel a vírusvektor beépíti a CAR gént a gazda T-sejt genomjában lévő tumorszuppresszorba vagy onkogénbe. Egyes retrovirális (RV) vektorok alacsonyabb kockázatot hordoznak, mint a lentivírus (LV) vektorok. Mindkettőnek azonban megvan a lehetősége, hogy onkogén. A T-sejtekben a CAR inszerciós helyek genomiális szekvenálási analízisét létrehozták a CAR T-sejtek funkciójának és in vivo perzisztenciájának jobb megértése érdekében.
Citokin felszabadulási szindróma
A CAR-T sejtekkel végzett kezelés után a leggyakoribb probléma a citokin felszabadulási szindróma (CRS), egy olyan állapot, amelyben az immunrendszer aktiválódik, és megnövekedett számú gyulladásos citokin szabadul fel. Ennek a szindrómának a klinikai megnyilvánulása a szepszishez hasonlít magas lázzal, fáradtsággal, izomfájdalmakkal, hányingerrel, kapilláris szivárgással, tachycardiával és más szívműködési zavarokkal, májelégtelenséggel és vesekárosodással. A CRS szinte minden CAR-T sejtterápiával kezelt betegnél előfordul; Valójában a CRS jelenléte egy diagnosztikai marker, amely azt jelzi, hogy a CAR-T sejtek rendeltetésszerűen működnek a rákos sejtek elpusztítására. Megjegyzendő azonban, hogy a CRS súlyosságának magasabb fokozata nem a kezelésre adott megnövekedett válaszreakcióval, hanem inkább a magasabb betegségteherrel korrelál.
Immun effektor sejtekkel kapcsolatos neurotoxicitás
A neurológiai toxicitás gyakran társul a CAR-T sejt kezeléssel is. A mögöttes mechanizmus rosszul ismert, és lehet, hogy a CRS-hez kapcsolódik, de lehet, hogy nem. A klinikai megnyilvánulások közé tartozik a delírium, a koherens beszéd képességének részleges elvesztése, miközben továbbra is képes értelmezni a nyelvet (kifejező afázia), csökkent éberség (tompítottság) és görcsrohamok. Egyes klinikai vizsgálatok során neurotoxicitás okozta halálesetek fordultak elő. A neurotoxicitás okozta halálozás fő oka az agyödéma. A Juno Therapeutics, Inc. által végzett vizsgálatban öt, a vizsgálatba bevont beteg meghalt agyödéma következtében. A betegek közül kettőt önmagában ciklofoszfamiddal, a fennmaradó hármat ciklofoszfamid és fludarabin kombinációjával kezelték. Egy másik, a Fred Hutchinson Cancer Research Center által szponzorált klinikai vizsgálatban egy visszafordíthatatlan és végzetes neurológiai toxicitást jelentettek 122 nappal a CAR-T sejtek beadása után.