| Alfa-amiláz | |||||||||
|---|---|---|---|---|---|---|---|---|---|
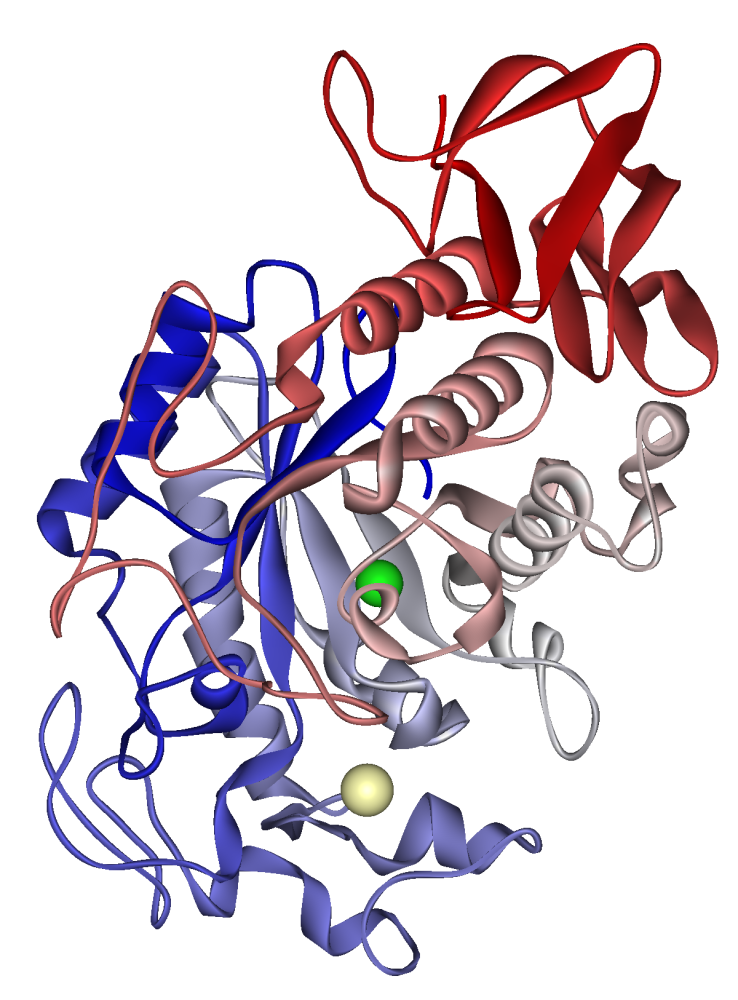
Humán nyálamiláz: halvány khaki színben látható kalciumion, zöld színben kloridion. EKT 1 SMD
|
|||||||||
| Azonosítók | |||||||||
| EK sz. | 3.2.1.0 | ||||||||
| CAS sz. | 9000-90-2 | ||||||||
| Adatbázisok | |||||||||
| IntEnz | IntEnz nézet | ||||||||
| BRENDA | BRENDA bejegyzés | ||||||||
| ExPASy | NiceZyme nézet | ||||||||
| KEGG | KEGG bejegyzés | ||||||||
| MetaCyc | anyagcsere út | ||||||||
| PRIAM | profil | ||||||||
| EKT struktúrák | RCSB PDB PDBe PDBsum | ||||||||
|
|||||||||
| GH13 katalitikus domén | |||||||||
|---|---|---|---|---|---|---|---|---|---|

Ciklodextrin-glükanotranszferáz (ec2.4.1.19) (cgtáz)
|
|||||||||
| Azonosítók | |||||||||
| Szimbólum | Alfa-amiláz | ||||||||
| Pfam | PF00128 | ||||||||
| Pfam klán | CL0058 | ||||||||
| InterPro | IPR006047 | ||||||||
| SCOP2 | 1ppi / SCOPe / SUPFAM | ||||||||
| OPM szupercsalád | 117 | ||||||||
| OPM fehérje | 1wza | ||||||||
| CAZy | GH13 | ||||||||
| CDD | cd11338 | ||||||||
|
|||||||||
| Alfa-amiláz C-terminális béta-lemez domén | |||||||||
|---|---|---|---|---|---|---|---|---|---|

Az árpa alfa-amiláz izozim 1 (amy1) inaktív d180a mutánsának kristályszerkezete maltoheptaózzal komplexben
|
|||||||||
| Azonosítók | |||||||||
| Szimbólum | Alfa-amil_C2 | ||||||||
| Pfam | PF07821 | ||||||||
| InterPro | IPR012850 | ||||||||
|
|||||||||
| Alfa-amiláz, C-terminális all-béta domén | |||||||||
|---|---|---|---|---|---|---|---|---|---|
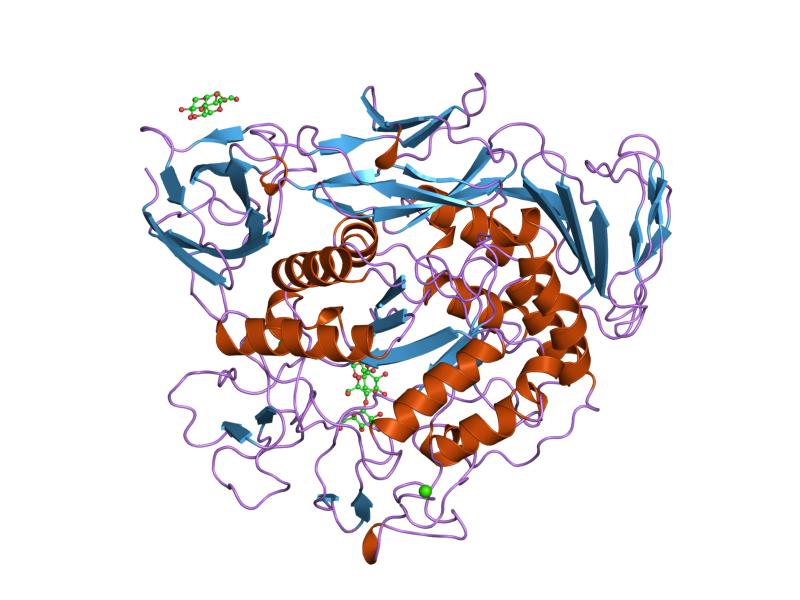
előkondicionált ciklodextrin glikoziltranszferáz mutáns maltotrióz komplexe
|
|||||||||
| Azonosítók | |||||||||
| Szimbólum | Alfa-amiláz_C | ||||||||
| Pfam | PF02806 | ||||||||
| Pfam klán | CL0369 | ||||||||
| InterPro | IPR006048 | ||||||||
| SCOP2 | 1ppi / SCOPe / SUPFAM | ||||||||
|
|||||||||
Alfa-amiláz, (α-amiláz) az EC 3.2.1.1 enzim, amely nagy, alfa-kapcsolt poliszacharidok, például keményítő és glikogén alfa-kötéseit hidrolizálja, és ezek rövidebb láncait, dextrineket és maltózt eredményez. Ez az amiláz fő formája, amely emberekben és más emlősökben található. A keményítőt tartalmazó magvakban is jelen van tápláléktartalékként, és számos gomba választja ki. A 13-as glikozid-hidroláz család tagja.
Az emberi biológiában
Bár sok szövetben megtalálható, az amiláz a legjelentősebb a hasnyálmirigy-nedvben és a nyálban, amelyek mindegyikének megvan a maga emberi α-amiláz izoformája. Különbözően viselkednek izoelektromos fókuszáláskor, és specifikus monoklonális antitestek felhasználásával a tesztelés során is elkülöníthetők. Emberben minden amiláz izoforma kapcsolódik az 1p21 kromoszómához (lásd AMY1A).
nyál amiláz (ptyalin)
Az amiláz a nyálban található, és a keményítőt maltózra és dextrinre bontja. Az amiláz ezen formáját ptyalinnak is nevezik. /ˈtaɪəlɪn/, amelyet Jöns Jacob Berzelius svéd kémikus nevezett el. A név a görög πτυω (köpök) szóból származik, mivel az anyagot nyálból nyerték. A nagy, oldhatatlan keményítőmolekulákat oldható keményítőkre (amilodextrinre, eritrodextrinre és achrodextrinre) bontja, így kisebb keményítőket és végső soron maltózt termel. A ptyalin lineáris α(1,4) glikozid kötésekre hat, de a vegyület hidrolíziséhez olyan enzimre van szükség, amely az elágazó termékekre hat. A nyál amilázt a gyomorban a gyomorsav inaktiválja. A pH 3,3-ra beállított gyomornedvben a ptyalin 37 °C-on 20 perc alatt teljesen inaktiválódott. Ezzel szemben az amiláz aktivitás 50%-a megmaradt 150 perces gyomornedvnek való kitettség után pH 4,3-on. Mind a keményítő, a ptyalin szubsztrátja, mind a termék (rövid láncú glükóz) képes részben megvédeni azt a gyomorsav általi inaktivációtól. A pufferhez 3,0 pH-értéken hozzáadott ptyalin 120 perc alatt teljesen inaktiválódik; azonban 0,1%-os keményítő hozzáadása az aktivitás 10%-át eredményezte, és 1,0%-os szinthez hasonló keményítő hozzáadása az aktivitás körülbelül 40%-át eredményezte 120 percnél.
Optimális feltételek a ptyalin számára
- Optimális pH – 7,0
- Az emberi test hőmérséklete
- Bizonyos anionok és aktivátorok jelenléte:
- Klorid és bromid – a leghatékonyabb
- Jodid – kevésbé hatékony
- Szulfát és foszfát – a legkevésbé hatékony
Az emberi nyál-amiláz genetikai változásai
A nyál amiláz génje megkettőződésen ment keresztül az evolúció során, és a DNS-hibridizációs vizsgálatok azt mutatják, hogy sok egyednél a gén többszörös tandem ismétlődése van. A génmásolatok száma korrelál a nyál amiláz szintjével, amit protein blot assay-vel mértek humán amiláz elleni antitesteket alkalmazva. A génkópiaszám a magas keményítőtartalmú étrendnek való látszólagos evolúciós expozícióhoz kapcsolódik. Például egy japán egyénnek 14 kópiája volt az amiláz génből (egy allél 10 kópiával és egy második allél négy kópiával). A japán étrend hagyományosan nagy mennyiségű rizskeményítőt tartalmazott. Ezzel szemben egy Biaka egyén hat másolatot hordozott (minden allélon három példány). A Biakák esőerdei vadászó-gyűjtögetők, akik hagyományosan alacsony keményítőtartalmú étrendet fogyasztanak. Perry és munkatársai azt feltételezték, hogy a nyál-amiláz gén megnövekedett kópiaszáma megnövelte a túlélést, ami egybeesett a keményítőtartalmú étrendre való átállással az emberi evolúció során.
Hasnyálmirigy amiláz
A hasnyálmirigy α-amiláza véletlenszerűen hasítja az amilóz α(1-4) glikozid kötéseit, így dextrint, maltózt vagy maltotriózt eredményez. Kettős elmozdulási mechanizmust alkalmaz az anomer konfiguráció megtartásával. Az emberekben a nyál amiláz annak másolatából fejlődött ki.
A patológiában
Az amiláz-teszt könnyebben elvégezhető, mint a lipáz-teszt, így ez az elsődleges teszt a hasnyálmirigy-gyulladás kimutatására és monitorozására. Az orvosi laboratóriumok általában vagy a hasnyálmirigy-amilázt, vagy a teljes amilázt mérik. Ha csak a hasnyálmirigy-amilázt mérik, a növekedés nem figyelhető meg mumpsz vagy más nyálmirigy-sérülés esetén.
A jelenlévő kis mennyiség miatt azonban az időzítés kritikus fontosságú, amikor ehhez a méréshez vérmintát vesznek. A hasnyálmirigy-gyulladásos fájdalom rohama után nem sokkal vért kell venni, különben gyorsan kiürül a vesén keresztül.
A nyál α-amilázt a stressz biomarkereként és a szimpatikus idegrendszer (SNS) aktivitásának helyettesítő markereként használták, amelyhez nincs szükség vérvételre.
Értelmezés
Emberben megnövekedett plazmaszintek a következők:
- Nyáltrauma (beleértve az érzéstelenítő intubációt is)
- Mumpsz – a nyálmirigyek gyulladása miatt
- Pancreatitis – az amilázt termelő sejtek károsodása miatt
- Veseelégtelenség – a csökkent kiválasztás miatt
A normálérték felső határának (ULN) több mint 10-szerese az összes amiláz érték hasnyálmirigy-gyulladásra utal. A felső határérték 5-10-szerese ileust, nyombélbetegséget vagy veseelégtelenséget jelezhet, és az alacsonyabb emelkedést általában nyálmirigy-betegségben észlelik.
Gének
- nyál- AMY1A, AMY1B, AMY1C
- hasnyálmirigy – AMY2A, AMY2B
Gabonában
A gabonában az α-amiláz aktivitást például a Hagberg–Perten esési számmal, a csírák károsodásának felmérésére szolgáló teszttel vagy a Phadebas módszerrel mérik. Búzában fordul elő.
Ipari felhasználás
Az α-amilázt az etanolgyártásban használják a gabonákban lévő keményítők fermentálható cukrokká történő felosztására.
A magas fruktóztartalmú kukoricaszirup előállításának első lépése a kukoricakeményítő α-amilázzal történő kezelése, amely rövidebb cukor-oligoszacharid-láncokat állít elő.
A „Termamyl” nevű α-amiláz, amelyet innen származik Bacillus licheniformisegyes mosószerekben is használatos, különösen a mosogató- és keményítőeltávolító tisztítószerekben.
Lásd az amilázt az amilázcsalád további felhasználásaiért általában.
Orvosi felhasználási lehetőség
Az α-amiláz hatékonynak bizonyult a polimikrobiális bakteriális biofilmek lebontásában azáltal, hogy hidrolizálja az α(1-4) glikozid kötéseket az extracelluláris polimer anyag (EPS) szerkezeti, mátrix exopoliszacharidjain belül.
Puffer gátlás
A trisz-molekula a jelentések szerint számos bakteriális α-amilázt gátol, ezért nem szabad trisz-pufferben használni.
Meghatározás
Számos módszer áll rendelkezésre az α-amiláz aktivitás meghatározására, és a különböző iparágak általában eltérő módszereket alkalmaznak. A keményítő-jód-teszt, a jódteszt továbbfejlesztése, a színváltozáson alapul, mivel az α-amiláz lebontja a keményítőt, és számos alkalmazásban használják. Hasonló, de iparilag előállított teszt a Phadebas amiláz teszt, amelyet minőségi és mennyiségi tesztként használnak számos iparágban, például mosó- és tisztítószerek, különféle liszt-, gabona- és malátaélelmiszerek, valamint a törvényszéki biológia területén.
Domain architektúra
Az α-amilázok számos különböző fehérjedomént tartalmaznak. A katalitikus domén szerkezete egy nyolcszálú alfa/béta hordóból áll, amely tartalmazza az aktív helyet, megszakítva egy ~70 aminosavból álló kalciumkötő doménnel, amely a béta 3. szál és az alfa hélix 3 között kinyúlik, és egy karboxil-terminális görög doménből áll. kulcsfontosságú béta-hordó tartomány. Számos alfa-amiláz tartalmaz egy béta-lemez domént, általában a C-terminálison. Ez a tartomány ötszálú antiparallel béta-lapként van felszerelve. Számos alfa-amiláz tartalmaz egy béta-domént, általában a C-terminálison.







Discussion about this post