Összegzés
- A kutatók egereken kezelték a sarlósejtes betegséget a betegséget okozó hibás hemoglobin gén közvetlen szerkesztésével.
- Ezek az eredmények a sarlósejtes betegség egyszeri kezeléséhez vezethetnek, kevesebb mellékhatással, mint más fejlesztés alatt álló kezelési módszerek.
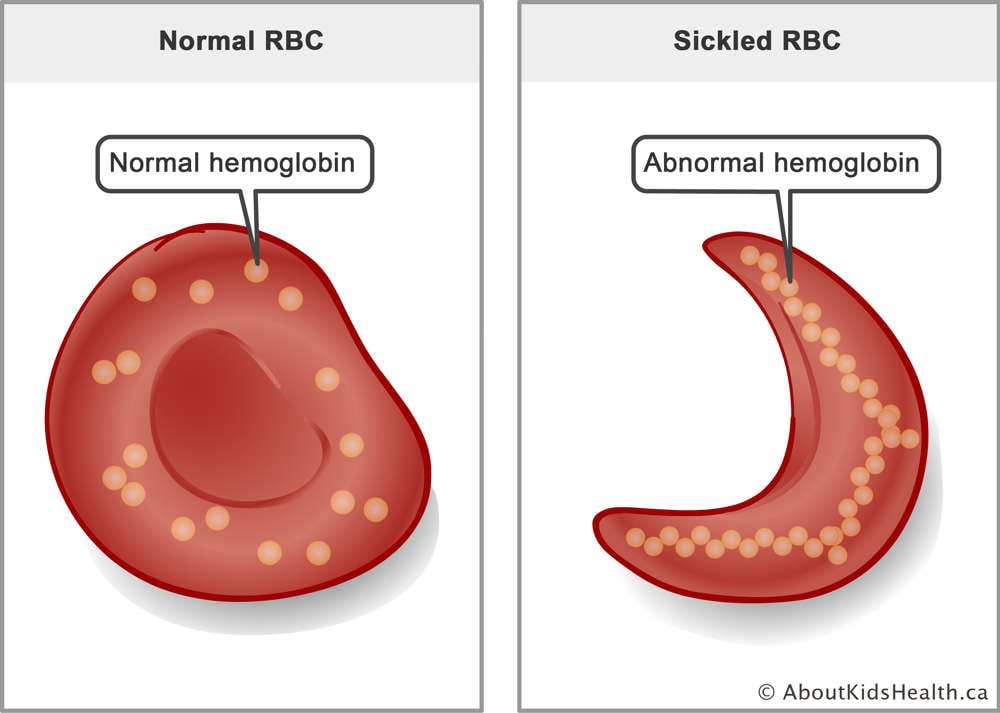
A sarlósejtes betegség (SCD) egy genetikai rendellenesség, amelyet egy személy HBB génjének mindkét másolatában bekövetkező mutáció okoz. Ez a gén a hemoglobin egy komponensét kódolja, amely a vörösvérsejtek oxigénszállító fehérje. A mutáció hatására a hemoglobin molekulák összetapadnak, sarló alakú vörösvértesteket hozva létre. Ez a folyamat vérsejt-repedéshez, vérszegénységhez, visszatérő fájdalomhoz, immunhiányhoz, szervkárosodáshoz és korai halálhoz vezethet. A csontvelő-transzplantáció meg tudja gyógyítani az SCD-t, de nehéz megfelelő donort találni. A transzplantációs eljárás veszélyes mellékhatások kockázatával is jár.
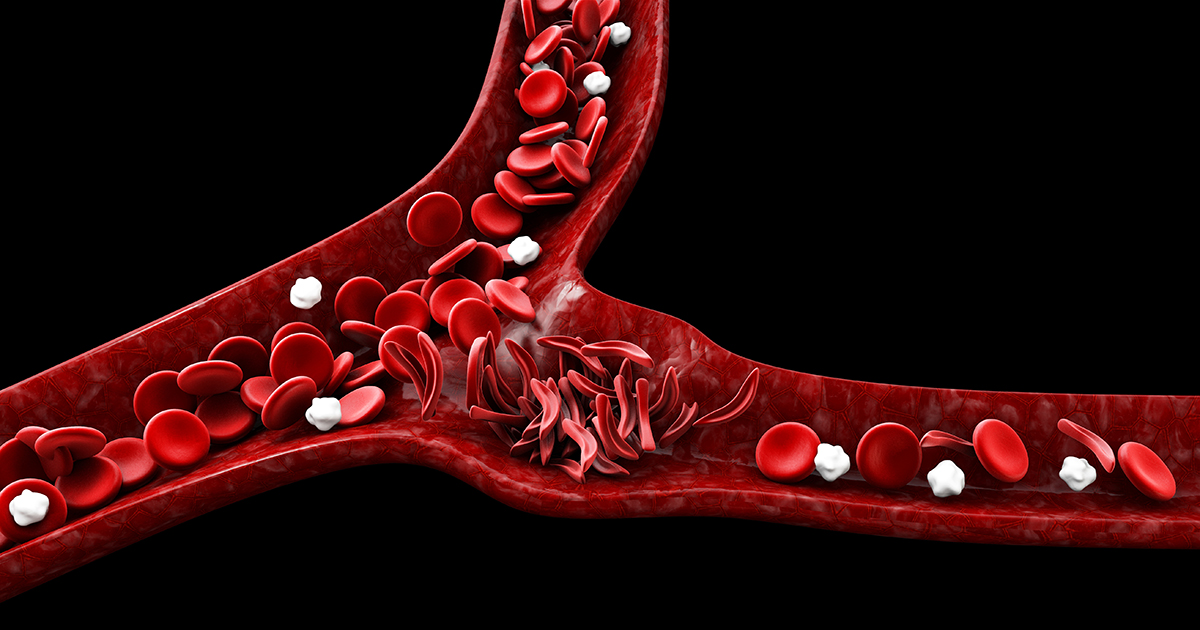
A sarlósejtes kórkép számos új kezelési módszere jelenleg fejlesztés alatt áll. Ezek a módszerek magukban foglalják a páciens saját csontvelősejtjeinek génszerkesztését, hogy normálisan működő hemoglobint állítsanak elő. Ezek a kezelési módszerek elkerülik a csontvelő-átültetésekkel kapcsolatos kockázatokat. De ezek a módszerek saját kockázatokat is hordoznak magukban, mivel új DNS bejuttatását és meglévő DNS-szálak hasítását foglalják magukban.
Dr. David Liu (a Broad Institute munkatársa, Dr. Mitchell Weiss és Dr. Jonathan Yen a St. Jude Gyermekkórházban az Egyesült Államokban) által vezetett kutatócsoport olyan módszert fejlesztett ki, amely elkerüli az egyéb génszerkesztési módszerek kockázatait. Ez a módszer a bázisszerkesztésnek nevezett molekuláris technikát alkalmazza, amely megváltoztatja a genom egyetlen betűjét anélkül, hogy bármilyen DNS-t levágna.
Sarlósejtes betegségben a T helyettesíti az A-t a HBB gén kulcsfontosságú helyén. Míg az alapszerkesztés nem tudja visszafordítani ezt a változást, a T-t C-vé alakíthatja. Ez a hatás a hemoglobin természetben előforduló, nem patogén variánsát, a Hb-Makassar nevű változatát hozza létre. A kutatók egy adenin bázisszerkesztőnek nevezett molekuláris eszközt terveztek, amely felismeri a gén mutáns részét, és a T-t C-vé alakítja.
A kutatók az adenin bázisszerkesztőt használták emberi SCD-betegek vérképző őssejtekén. A sejtek legfeljebb 80%-ában a sarlósejtes hemoglobin gén Makassar variánssá alakult át. Tesztelés céljából a csapat a szerkesztett emberi sejteket SCD egérmodelljébe ültette át. A transzplantáció után 16 héttel a donorból származó őssejtek 68%-ában voltak Hb-Makassarra szerkesztett HBB gének. Az ezekből az őssejtekből származó vörösvérsejtek jelentősen csökkentették a sarlósodást.
Mivel az emberi vörösvérsejtek nem tudnak elég sokáig életben maradni egerekben a kiterjedt teszteléshez, a csapat ezután egy egér SCD-modellből vett őssejteket, szerkesztette azokat, és átültette a szerkesztett sejteket egy másik egércsoportba. 16 hét elteltével a Makassar-variáns a recipiens egerek hemoglobinjának csaknem 80%-át tette ki. A nem szerkesztett sejteket kapott kontroll egereknek jellegzetes SCD tünetei voltak: vérszegénység, rendellenes vérsejtszám, sarló alakú vörösvértestek és megnagyobbodott lép. A módosított őssejteket kapott egerek tünetei nagymértékben javultak.
A kutatók csontvelőt vettek azoktól az egerektől, amelyek megkapták a szerkesztett őssejteket, és átültették egy új egércsoportba. Az új recipiensek vérsejtszáma egészséges volt, ami megerősíti a génszerkesztés tartósságát. A kutatók azt is megállapították, hogy az SCD génmásolatok legalább 20%-ának szerkesztése elegendő az egészséges vérmérések fenntartásához. Nem észleltek semmilyen mellékhatást az egereknél a génszerkesztési folyamatból.
„A megközelítés ígéretet kínál a sarlósejtes betegség egyszeri kezelésének, vagy akár egyszeri gyógyításának alapjaként” – mondja Liu.
A csapat jelenleg a koncepció továbbfejlesztésén dolgozik, azzal a végső céllal, hogy elérje a betegeket.







Discussion about this post