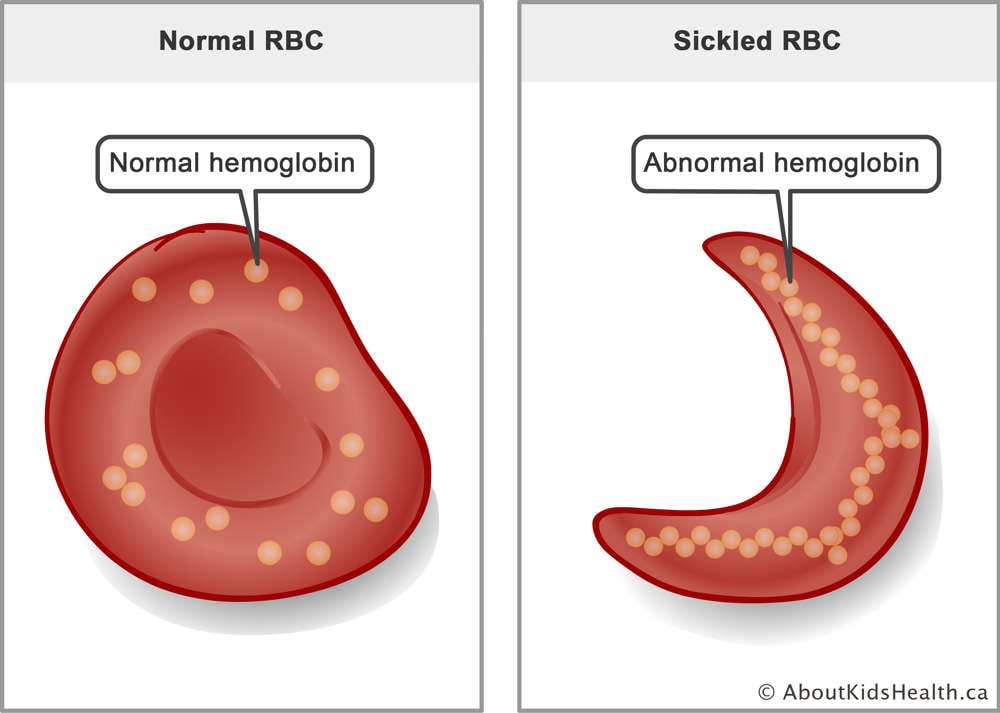
Az akut limfocitás leukémia (ALL) a leukémia négy fő típusának egyike.
Az „akut” azt jelenti, hogy kezelés nélkül gyorsan fejlődik. A „limfocita” limfocitákra, éretlen fehérvérsejtekre utal. Az Egyesült Államokban körülbelül 4000 embernél diagnosztizálnak ALL-t
A Philadelphia kromoszóma (Ph+) ALL az ALL egy specifikus típusa, amelyet a Philadelphia kromoszómának nevezett genetikai mutáció jellemez.
Annak ellenére, hogy MINDEN az
Ez a ritka állapot számos más néven is szerepel, beleértve a Ph+ vagy PH+ akut limfoblaszt leukémiát.
Olvassa tovább, hogy többet megtudjon a Ph+-ról, beleértve azt is, hogy miben különbözik az ÖSSZES típustól, kockázati tényezőkről és kezelési lehetőségekről.
Mi is pontosan az a Philadelphia Chromosome ALL?
A Ph+ az ALL egyik altípusa, ahol a leukémiás sejtek a felfedezés helyéről elnevezett Philadelphia kromoszómának nevezett genetikai mutációt tartalmaznak. A más típusú ALL-ban szenvedőknek nincs meg ez a kromoszómája.
Az emberi sejtekben általában 23 pár kromoszóma van, amelyek genetikai információkat tartalmaznak. A Philadelphia kromoszóma egy rövidített változata
A BCR-ABL egy tirozin-kináz nevű fehérjét termel. Ez a fehérje a leukémiás sejtek kontrollálatlan növekedését okozza, és kiszorítja az egészséges fehérvérsejteket.
A Ph+-os emberekkel együtt
Számos genetikai mutációt azonosítottak az ALL bármelyik típusában szenvedő emberekben, például:
- hiányzó 7-es kromoszóma
- egy extra 8-as kromoszóma
- kóros változások a 4-es és 11-es kromoszómák génjeiben
- a szokásosnál kevesebb kromoszóma
- a szokásosnál több kromoszóma
- kóros változások a 10. és 14. kromoszómák génjeiben
Ph-pozitív vs. Ph-negatív
Ha a Philadelphia kromoszómák nincsenek jelen, a betegséget Ph-negatív (Ph-) ALL néven ismerik. Az ALL típusának meghatározása segíthet az orvosnak meghatározni a prognózisát és a legjobb kezelési lehetőségeket.
A Ph+ megszerzését hagyományosan kevésbé pozitív kilátásokkal társították. De a tirozin-kináz-gátlóknak (TKI-k) nevezett célzott terápia közelmúltbeli fejlesztése javította a kilátásokat. A kezelés általában kevésbé hatékony a 60 év feletti felnőtteknél.
Ph-szerű MINDEN
Egy másik, Ph-szerű ALL altípus háromszor gyakoribb, mint a Ph+.
Az ilyen altípusú embereknél hiányzik a BCR-ABL génmutáció, de a rák hasonlóan viselkedik.
Hogyan tudok tesztelni?
Miután diagnosztizálták Önnél az ALL-t, az egészségügyi szakember speciális vizsgálatokat végezhet annak megállapítására, hogy melyik altípussal rendelkezik.
Egy kis vérmintát laboratóriumban elemeznek. Valószínűleg csontvelő-aspirációt és biopsziát fognak végezni. Ez úgy történik, hogy kis csontvelőmintát veszünk ki, általában a csípőből.
Ezután a minták elemzéséhez többféle laboratóriumi vizsgálat egyike használható:
- Citogenetika. A hagyományos citogenetikában a DNS-t mikroszkóp alatt elemzik, hogy megvizsgálják a sejtek osztódását.
- Fluoreszcens in situ hibridizációs (FISH) teszt. Ez a teszt speciális fluoreszcens festékeket használ a BCR-ABL gén azonosítására. Ezek a színezékek bizonyos génekhez kötődnek, másokhoz nem.
- Polimeráz láncreakció (PCR) teszt. A PCR teszt még kis mennyiségű Philadelphia kromoszómát is képes kimutatni, amely más tesztekkel nem azonosítható.
Melyek a leggyakoribb kockázati tényezők?
A gyermekeknél nagyobb valószínűséggel diagnosztizálnak ALL-t – és a felnőtteknél az ALL esetek mindössze 25%-ában diagnosztizálnak Ph+-t.
MINDEN van
- hímek, mint nőstények
- fehérek, mint az afroamerikaiak
Néhány
- benzolnak való kitettség olyan anyagokban, mint a fényvédő
- ionizáló sugárzás
- korábbi kemoterápia és sugárterápia
ALL gyakrabban fordul elő olyan gyermekeknél, akiknél ilyen állapotok vannak:
- Down-szindróma
- neurofibromatózis
- Bloom szindróma
- ataxia-telangiectasia
Milyen kezelési lehetőségek állnak rendelkezésemre?
A Ph+ kezelése általában a TKI-nek nevezett célzott terápiából és vegyes kemoterápiás rendszerből áll. Ezután egy allogén csontvelő-transzplantáció következik.
Ez a fajta transzplantáció úgy történik, hogy olyan donortól vesznek csontvelősejteket, aki genetikailag közeli rokonságban áll Önnel, és a sejteket a csontvelőbe ültetik át, hogy pótolják a sérült sejteket. A
A TKI-k blokkolják a BCR-ABL fehérje azon képességét, hogy olyan jeleket küldjenek, amelyek leukémiás sejtek kialakulásához vezetnek. Az imatinib a leggyakrabban használt TKI. Dasatinib és ponatinib is használatos. Egy klinikai vizsgálat a ponatinib és az imatinib hatékonyságát vizsgálja.
A Ph+ kilátásai a TKI-k használata óta javultak. Mielőtt a TKI-k elérhetőek lettek volna, a kemoterápiában részesülő Ph+-os felnőttek 3 éves teljes túlélési aránya kisebb volt, mint
Az American Journal of Cancer Research 2015-ös tanulmánya megállapította, hogy a TKI imatinibbel kombinált kemoterápia több mint 90 százalékra emelte a felnőtteknél a remisszió arányát – vagyis a rák teljesen megszűnt –, és az 5 éves teljes túlélési arányt 43 százalékra.
A kemoterápia ALL esetében általában kb
Milyenek a kilátások?
A Ph+ diagnózis kezelése nehéz lehet, de a TKI-k alkalmazása jelentősen javította a kilátásokat.
A gyerekeknek általában nagyobb az esélye a túlélésre, de mindenki túlélési aránya növekszik. 30 évesnél fiatalabb, és fehérvérsejtszáma kevesebb, mint
A legtöbb Ph+-os gyermeket sikeresen kezelik
A
| Leírás | Mérték |
| Általános túlélési arány | 74,1% |
| Túlélési arány komplikációk nélkül öt év után | 54,2% |
| Öt év elteltével a halál teljes kockázata | 25,9% |
| A visszaesés általános kockázata (a tünetek a kezelés után ismét súlyosbodnak) | 30% |
Kérdezze meg egészségügyi szakemberét azokról a klinikai vizsgálatokról, amelyekre jogosult lehet. Egyes klinikai vizsgálatok olyan korszerű kezelésekhez biztosítanak hozzáférést, amelyek egyébként nem lennének elérhetőek.